01. (FPS) Vacinas de DNA são definidas como preparações purificadas de plasmídeos, contendo uma ou mais sequências de DNA, capazes de induzir resposta imune contra patógenos. Tal imunidade é conferida porque ocorre:
a) transcrição de genes de interesse no interior das células dos microrganismos alvo.
b) produção de anticorpos pelo hospedeiro capazes de reconhecer genes de microrganismos.
c) síntese de proteínas microbianas pelas células do hospedeiro, estas atacadas pelo sistema imune.
d) reconhecimento pelo sistema imune de proteínas nos microrganismos alvo.
e) reconhecimento de microrganismos por anticorpos no interior das células do hospedeiro.
02. (UCS) “As mulheres nascem com um determinado número de óvulos”. Essa máxima perdurou por muito tempo implicando em um período restrito de fertilidade em função do envelhecimento dessas células e, consequentemente, acarretando problemas na gravidez e no feto. A ciência, em 2004, descobriu as células-tronco ovarianas (CTOs), o que significa uma nova revolução reprodutiva. Sobre o enunciado acima, é correto afirmar que:
a) as mulheres nascem com um número determinado de células, pois todas suas ovogônias iniciam sua meiose no período embrionário, formando ovócitos II.
b) a identificação de CTOs impossibilita a mulher desenvolver células jovens para a reprodução que podem ser retiradas em qualquer fase do ciclo reprodutivo.
c) uma das implicações associadas à idade dos óvulos são as doenças e síndromes, que não seriam evitadas, pois a mulher já possui a predisposição.
d) a síndrome de Down apresenta uma relação de 1 caso para 700 nascimentos; como é uma doença genética, as CTOs não ajudariam neste caso.
e) a técnica mais recomendada atualmente para evitar gravidez de risco é a retirada de óvulos de mulheres em idade fértil, para posterior fecundação.
03. (UDESC) “Um número crescente de clínicas, muitas vezes em países como a Rússia ou a China, mas também na Europa e outros continentes, afirmam em seus sites que podem tratar e até curar doenças como distrofia muscular, Alzheimer, Parkinson e lesão na coluna vertebral, assim como infartos, injetando nos pacientes células-tronco que, em teoria, podem se transformar em um nervo, um músculo ou outras células e reparar danos causados por uma doença ou lesão. Relatos de atletas sobre resultados aparentemente miraculosos contribuem para um interesse crescente. Estima-se que dezenas de milhares de pacientes ao redor do mundo tenham recorrido a tais tratamentos e que o setor movimente centenas de milhões de dólares”.
Analise as proposições em relação às células tronco, e assinale (V) para verdadeira e (F) para falsa.
( ) O uso das células tronco em terapias baseia-se no princípio de que elas podem gerar qualquer tipo de célula.
( ) Os mecanismos genéticos, que promovem a diferenciação celular, já são suficientemente conhecidos para assegurar a correta transformação das células tronco naquelas que o paciente necessita.
( ) Não existe o risco destas células se transformarem em tumores.
( ) Todas as células, independentemente do seu grau de diferenciação, podem ser transformadas em células tronco.
Assinale a alternativa que indica a sequência correta, de cima para baixo.
a) V – F – V – V.
b) F – V – F – F.
c) V – F – F – F.
d) F – V – V – V.
e) F – F – F – V.
04. (UPE) Leia o texto a seguir:
Atualmente, o gene considerado como o mais confiável para discriminar se um atleta tem mais força ou resistência é o ACTN3, apelidado gene da velocidade. Localizado no cromossomo 11, o ACTN3 é responsável pela produção da proteína alfa actinina 3, ativada exclusivamente em fibras musculares de contração rápida. Uma alteração em uma única base nitrogenada faz que esse gene possa apresentar duas formas na população humana: a versão “normal”, funcional, denominada R, que produz alfa actinina 3; e a variante alterada, chamada X, em que a tal proteína não é sintetizada. O gene ACTN3 assim como a eritropoietina (EPO), hormônio do crescimento humano (hGH), inibidor de genes da miostatina, endorfina, encefalina, leptina, dentre outros, são possíveis alvos primários do doping genético em humanos, por meio de terapia gênica in vivo, na qual o processo de transgenia ocorre dentro do indivíduo, ou ex vivo, no qual parte do engenheiramento genético ocorre fora do corpo, e parte, dentro.
Sobre ele, é correto afirmar que:
a) corredores de longa distância tendem a possuir, ao menos, uma cópia da variante R, a forma funcional, do gene ACTN3. A menor quantidade da proteína melhoraria o desempenho dos atletas em tarefas que dependem da ação das fibras rápidas.
b) corredores velocistas precisam ser resistentes ao cansaço e tendem a ser XX quanto ao gene ACTN3. A ausência parcial da proteína levaria o organismo a se adaptar melhor a exercícios de longa duração que retiram energia do consumo de oxigênio.
c) o doping genético é considerado o uso terapêutico de células, genes e elementos gênicos que venham a aumentar o desempenho físico do atleta por meio de substâncias químicas e fármacos.
d) o doping genético ex vivo envolve a transferência de genes para células em meio de cultura e reintrodução para o tecido-alvo do atleta, o que aumentaria a expressão de hormônios e outras substâncias bioquímicas, trazendo melhoria ao seu desempenho físico.
e) o princípio da terapia gênica in vivo consiste na transferência de proteínas e lipídeos para células-alvo por meio de pílulas, com o objetivo de suprir os produtos de um gene estruturalmente anormal no genoma do atleta.
05. (UEG) A pele, os epitélios intestinais e especialmente o sangue são estruturas presentes no organismo humano adulto que possuem a capacidade de regeneração por meio de um processo complexo e finamente regulado, visto que suas células são destruídas e renovadas constantemente. Esse processo de renovação se dá de forma geral conforme apresentado no esquema a seguir:
Com base nessas informações, verifica-se que
a) a hematopoiese resulta da diferenciação e proliferação simultânea das células-tronco que, à medida que se diferenciam, vão reduzindo sua potencialidade.
b) as diferentes linhagens hematopoiéticas geradas no sistema preservam altas taxas de proliferação e diferenciação.
c) existe um aumento gradual da capacidade de autorrenovação das células progenitoras durante esse processo.
d) células-tronco hematopoiéticas apresentam potencial para diferenciar-se em qualquer célula do corpo humano, todavia não geram outras células-tronco.
e) as células precursoras e maduras já diferenciadas são utilizadas em procedimentos de utilização de células-tronco no tratamento de alguma doença.
06. (UFMS) Pesquisadores brasileiros identificaram no café um gene com respostas adaptativas à escassez de água. Para confirmar a capacidade do gene, de proteção a seca, os pesquisadores clonaram o gene e o transferiram para outra espécie, Arabidopsis thaliana, que é utilizada como modelo em estudos genéticos. Com base nessas informações, considere as afirmativas a seguir.
I. Os pesquisadores usaram cruzamentos naturais para a transferência do gene de resistência à seca do café para Arabidopsis thaliana.
II. Os pesquisadores usaram a transgenia para a transferência do gene de resistência à seca do café para Arabidopsis thaliana.
III. As plantas de Arabidopsis thaliana que receberam o gene de resistência a seca, oriundo de plantas de café, são plantas transgênicas.
Está(ão) correta(s):
a) Apenas I.
b) Apenas II.
c) Apenas III.
d) Apenas II e III.
e) I, II e III.
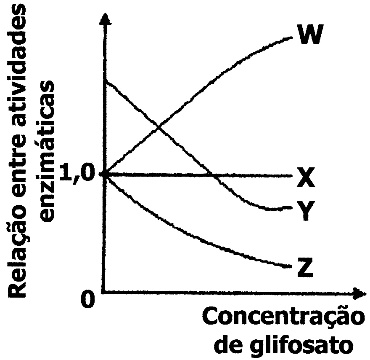
07. (UERJ) A enzima EPSP-sintase, presente em praticamente todos os vegetais, é modificada na soja transgênica, tornando-a resistente à inibição pelo herbicida glifosato. Assim, o tratamento com esse herbicida não prejudica o desenvolvimento de culturas de soja transgênica, mas evita o crescimento de outros vegetais indesejáveis. Num estudo para a identificação da variedade transgênica de soja, foi medida, nas mesmas condições experimentais, a atividade da EPSP-sintase em extratos de folhas de diferentes tipos desse vegetal, em presença ou ausência de glifosato. As atividades da enzima nesses extratos, na ausência do inibidor, apresentaram o mesmo valor. Observe o gráfico abaixo.
A curva que corresponde à razão entre as atividades de uma enzima da variedade transgênica e as atividades dessa mesma enzima da soja comum é a indicada pela seguinte letra:
a) W.
b) X.
c) Y.
d) Z.
08. (UEM) A terapia gênica consiste na inserção de genes normais humanos em células humanas. Alguns atletas se utilizam desta técnica para inserir em suas células genes que codificam fenótipos atléticos, gerando vantagens esportivas. Essa técnica é considerada doping e denominada doping genético. Com base nestas informações e em assuntos correlatos, assinale o que for correto.
01. Para se atingir o fenótipo atlético desejado, além da inserção do gene, é necessário o envolvimento de fatores adequados, tais como treinos físicos e nutrição.
02. Para se atingir o fenótipo atlético desejado, além da inserção do gene, é necessário que ocorra a expressão dos genes inseridos.
04. Para se atingir o fenótipo atlético desejado, é necessário inserir no genoma do atleta sequências de DNA que codifiquem RNA. Estes serão sintetizados pela enzima RNA polimerase e traduzidos pelos ribossomos.
08. O doping genético altera tanto o genótipo como o fenótipo do atleta dopado.
16. O processo descrito no comando da questão também pode ser definido como transgênese.
Soma das alternativas corretas:
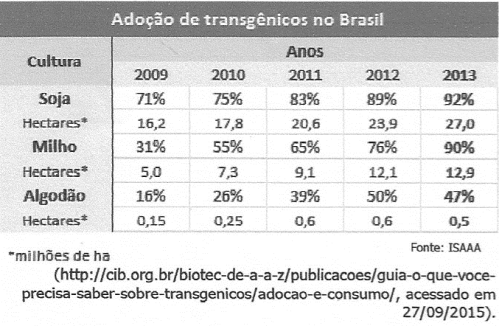
09. (UNESPAR) “No Brasil, foram plantados 40,3 milhões hectares com sementes de soja, milho e algodão transgênicos em 2013, com um crescimento de 10% em relação ao ano anterior. Esse desempenho levou o Brasil a consolidar a posição conquistada em 2009, o de segundo lugar no ranking de área plantada com transgênicos no mundo, ficando atrás apenas dos Estados Unidos”.
Sobre o assunto, assinale o que for correto.
a) A característica de interesse retirada de outro organismo de espécie diferente será manifestada em decorrência da transcrição do RNA transportador sintetizado a partir do DNA recombinante.
b) As enzimas de restrição empregadas na tecnologia de DNA recombinante são fundamentais porque permitem modificar sequências de bases nitrogenadas do DNA.
c) Diferentes variedades de milho podem ser obtidas com a utilização de outros genes, por meio da técnica denominada clonagem.
d) As sementes de soja, milho e algodão transgênicos são produzidas pela técnica do melhoramento genético vegetal convencional.
e) Através da tecnologia do DNA recombinante foi possível produzir plantas geneticamente modificadas com genes bacterianos que conferem resistência a pragas da lavoura.
10. (UPE) A era da biotecnologia, tal qual a revolução industrial, a revolução verde e a era da informação, promete grandes vantagens e benefícios à humanidade. Também tem gerado polêmicas e questionamentos acerca dos impactos que possam vir a causar ao homem e aos ecossistemas naturais. Com relação às características das técnicas utilizadas, ao papel desempenhado e aos processos que envolvem a biotecnologia, analise as afirmativas e conclua.
I II
0 0 – A terapia gênica e a clonagem são técnicas desenvolvidas pela engenharia genética. Na terapia gênica, genes alterados, cujas deficiências originam diversas doenças humanas, são substituídos por genes normais.
1 1 – Com a utilização de células-tronco, temos a possibilidade da cura de várias doenças humanas. Sua maior aplicação é na prevenção da eritroblastose fetal.
2 2 – O teste de paternidade é uma metodologia da biotecnologia segura, incluindo a análise do DNA ou o exame bioquímico de identificação dos grupos sanguíneos. Através de qualquer dos métodos, é possível provar que um homem é, de fato, pai de uma criança.
3 3 – Organismos transgênicos contêm genes de outras espécies, inseridos através de técnicas de Engenharia Genética. As mulas, híbridos resultantes do cruzamento entre o jumento Equuos asinos e a égua Equuos caballus, são exemplos de transgênicos.
4 4 – DNA fingerprint corresponde à “impressão digital” genética de um indivíduo. Cada ser humano possui uma composição genômica exclusiva.
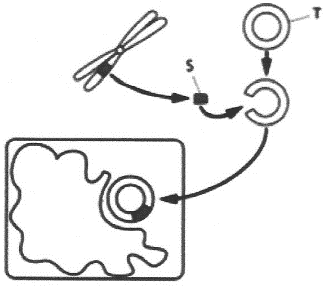
11. (FACTO) A insulina é um hormônio muito importante para o metabolismo humano, pois atua na regulação dos níveis de glicose no sangue. Pessoas que não produzem ou o fazem em quantidade insuficiente necessitam receber doses de insulina em concentrações adequadas. Uma forma de se produzir insulina é através da engenharia genética, onde por meio da técnica de DNA recombinante é possível produzir insulina utilizando microrganismos modificados. Na figura abaixo são representados os estágios na produção de uma substância como a insulina, através da engenharia genética.
Nas alternativas abaixo, marque a resposta que identifique respectivamente as letras S e T representadas na figura.
a) Cromossomo e plasmídeo.
b) Gene e bactéria.
c) Plasmídeo e gene.
d) Gene e plasmídeo.
e) Plasmídeo e cromossomo.
12. (UFLA) Organismos nos quais se tenham introduzido DNA de outra espécie ou DNA modificado da mesma espécie são chamados organismos geneticamente modificados ou transgênicos. Com base nisso, analise as proposições abaixo:
I. Entre os animais transgênicos, há aqueles com genes humanos para a produção de determinadas substâncias, tais como fatores para coagulação do sangue.
II. Uma das aplicações dos transgênicos é desenvolver animais em risco de extinção, com o animal se desenvolvendo no útero de outra espécie
III. Animais transgênicos transplantados com genes do hormônio do crescimento são utilizados para produzir carne menos gordurosa
IV. Com a transgenia é possível gerar um indivíduo inteiro a partir de um único animal que tenha alguma característica de interesse econômico.
É correto afirmar que são aplicações dos animais transgênicos:
a) Somente as proposições III e IV.
b) Somente as proposições II e IV.
c) Somente as proposições I e III.
d) Somente as proposições I e II.
13. (UFAM) Por meio da utilização de ferramentas de Biologia Molecular, é possível investigar comparativamente, perfis genéticos de amostras biológicas, visando à obtenção de informações valiosas sobre as diferenças entre essas amostras, em nível molecular. Para a investigação de paternidade, por exemplo, é realizada a extração de DNA das amostras coletadas, seguida da amplificação de regiões repetitivas (ex.: VNTRs) que, clivadas com enzimas de restrição, geram padrões únicos de polimorfismo para cada indivíduo. O gel de eletroforese permite a separação dos fragmentos de restrição conforme seu peso molecular, fornecendo o perfil eletroforético dos indivíduos que se deseja comparar. A figura a seguir ilustra os perfis eletroforéticos de 5 indivíduos envolvidos em um caso de investigação de paternidade: o filho (F), a mãe (M) e os prováveis pais: P1, P2 e P3:
Com base no enunciado da questão e no perfil eletroforético, assinale a alternativa incorreta:
a) A amplificação é optativa, porque as células da mucosa da boca fornecem DNA preservado, sendo possível obter perfis eletroforéticos confiáveis utilizando diretamente o DNA extraído em laboratório. De fato, os laboratórios de análise de DNA utilizam essa via rápida para reduzir despesa e tempo.
b) Amostras biológicas utilizadas para a realização dos testes de paternidade podem ser: células da mucosa da boca, sangue e cabelo. Esse último, desde que apresente o bulbo, que corresponde à região do folículo piloso que contém células viáveis.
c) O resultado do perfil eletroforético no enunciado mostra claramente que, mesmo sem considerar o perfil materno, o confronto do perfil do filho com os prováveis pais indicaria que apenas um deles teria chance de ser apontado como possível pai.
d) O resultado do perfil eletroforético mostra que, de todos os possíveis pais, P2 é aquele que apresenta maior divergência genética comparado a F.
e) Analisando as informações da questão, pode-se concluir que os testes de criminalística podem ser realizados utilizando a mesma ferramenta. No entanto, seria necessário confrontar o material biológico dos possíveis suspeitos com os vestígios de material biológico colhidos na cena do crime.
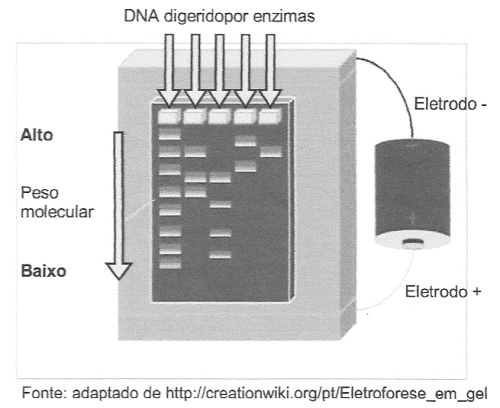
14. (FPS) A exposição do DNA humano a enzimas de restrição produz fragmentos que podem ser visualizados por meio de uma técnica denominada eletroforese, como ilustrado abaixo.
Neste caso, a identificação forense, por meio do DNA, é possível porque são produzidos fragmentos com padrões distinguíveis:
a) Entre os animais e a espécie humana.
b) Entre humanos, mesmo em irmãos univitelinos.
c) Em função do número de nucleotídeos.
d) De acordo com as sequências de nucleotídeos.
e) Em função dos tipos de nucleotídeos.
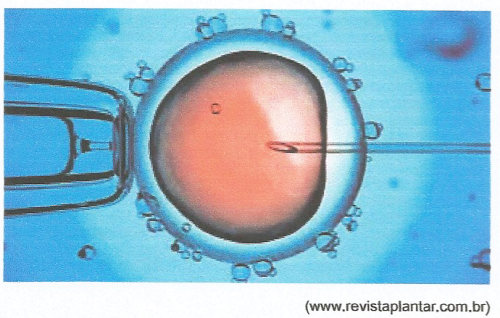
15. (UEA) A fotomicrografia mostra a introdução de um núcleo somático em um ovócito II, que se encontra preso por sucção a uma pipeta. O material genético está sendo introduzido no ovócito II por uma microinjeção intracitoplasmática.
O processo indicado na fotomicrografia permite a:
a) Produção de microrganismos transgênicos.
b) Clonagem de mamíferos.
c) Terapia gênica.
d) Obtenção de vacinas gênicas.
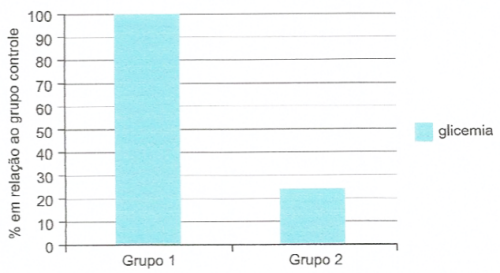
16. (UEA) Dois grupos de camundongos transgênicos foram submetidos à dosagem de glicose no sangue cerca de trinta minutos após as refeições. Os resultados foram comparados aos apresentados por um grupo controle de camundongos normais.
O gráfico permite concluir corretamente que:
a) Os camundongos dos grupos 1 e 2 têm uma cópia extra do gene responsável pela síntese da insulina.
b) Apenas os camundongos do grupo 1 têm uma cópia extra do gene responsável pela síntese do glucagon.
c) Os camundongos dos grupos 1 e 2 têm uma cópia extra do gene responsável pela síntese do glucagon.
d) Apenas os camundongos do grupo 1 têm uma cópia extra do gene responsável pela síntese da insulina.
e) Apenas os camundongos do grupo 2 têm uma cópia extra do gene responsável pela síntese da insulina.
17. (UNCISAL) As vacinas são classificadas em três grandes grupos (ou gerações) em razão das estratégias ou dos conceitos utilizados na preparação do princípio ativo […]. Nas vacinas de primeira geração o agente patogênico é inativado ou atenuado. Nesse grupo, destacam-se vacinas de prevenção da coqueluche, contra varíola, poliomielite, sarampo, rubéola, adenovírus […]. Na segunda geração, a indução de anticorpos é voltada para um único alvo, uma toxina, ou açúcares de superfície, que permite ao sistema imune neutralizar o agente infeccioso. Nesse grupo, destacam-se vacinas acelulares que empregam toxoides (toxinas purificadas e inativadas por tratamento químico), proteínas e polissacarídeos purificados, como as antitetânica, antidiftérica, hepatite B e as vacinas para o controle da meningite meningocócica e da pneumonia.
[…] Na terceira geração, o conceito vacinal surgiu da observação de células em que o DNA injetado conseguiu penetrar as membranas citoplasmática e nuclear e utilizar o maquinário enzimático necessário à transcrição e tradução, produzindo o antígeno que desencadeará uma série de respostas imunológicas. Embora as perspectivas depositadas nas vacinas de DNA tenham sido frustradas pela baixa imunogenicidade de diversas vacinas submetidas a testes clínicos, os resultados indicam que essas vacinas podem ser instrumentos excelentes para a ativação de respostas imunológicas citotóxicas e, consequentemente, controle de patógenos de replicação intracelular como vírus, algumas bactérias e certos tipos de câncer.
DINIZ, M.O. & FERREIRA, L.C.S. Biotecnologia aplicada ao desenvolvimento de vacinas. Estudos Avançados, v. 24, n. 70, 2010 (adaptado).
Dadas as afirmativas sobre a tecnologia do DNA recombinante na produção de vacinas:
I. As estratégias de clonagem e de introdução de mutações em genes específicos têm permitido a produção de vírus e bactérias inativos de forma mais precisa e segura do que os métodos convencionais das vacinas de primeira geração.
II. O aprimoramento das técnicas de produção de proteínas recombinantes, através de sistemas de expressão heterólogos, permite que bactérias, leveduras, células de mamíferos e insetos sejam utilizados para a produção de antígenos.
III. A tecnologia do DNA recombinante na produção de vacinas de DNA tem representado uma forma alternativa de desenvolver imunoterapias – vacinas com propriedades terapêuticas.
Verifica-se que está(ão) correta(s):
a) I, II e III.
b) I e III, apenas.
c) I e II, apenas.
d) III, apenas.
e) II, apenas.
18. (UEM) Uma nova estratégia para perder peso, baseada nas informações contidas no material genético de cada um, está ganhando espaço no Brasil e no mundo. Batizada de “dieta do DNA”, o método propõe ajudar decisivamente no emagrecimento por meio de análises das variações genéticas relacionadas à capacidade do corpo de reagir aos alimentos e ao treino físico. Ele fornece respostas a respeito da sensibilidade ao carboidrato e à gordura saturada e se há intolerância ao glúten e à lactose (Revista Isto É, 17/06/2015).
Sobre o assunto e com base nas aplicações do conhecimento genético, assinale a(s) alternativa(s) correta(s).
01. A dieta do DNA consiste em um método de transgenia.
02. Os resultados do Projeto Genoma Humano não oferecem nenhum avanço na identificação dos genes associados à obesidade.
04. A dieta do DNA é aceitável, pois as pessoas diferem entre si quanto ao material genético que possuem.
08. A análise do DNA, conhecida como fingerprint do DNA (impressão digital do DNA), é realizada cortando o DNA com enzimas de restrição e analisando por eletroforese.
16. A existência de diferenças genéticas entre os indivíduos de uma população é chamada de recombinação genética.
Soma das alternativas corretas:
19. (UPE) Leia o texto a seguir:
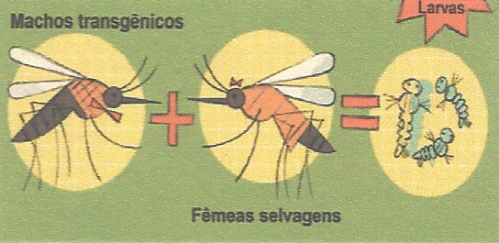
Um dos recursos existentes para o combate ao mosquito é o uso de inseticidas. O problema é que, por ser a estratégia mais utilizada, o Aedes aegypti desenvolveu resistência aos inseticidas mais comuns, à base de piretroides, e não se espanta com a maior parte dos repelentes. A ideia é encontrar estratégias para o controle de duas ou três gerações do inseto ao mesmo tempo e quebrar a sua dinâmica reprodutiva. Numa fábrica localizada em Juazeiro, na Bahia, Margareth Capurro, do ICB-USP, trabalhou com a Moscamed Brasil para implementar a produção de uma linhagem desenvolvida pela empresa britânica Oxford Insect Technologies (Oxitec). Esses mosquitos geneticamente alterados acumulam uma proteína, que faz as células das larvas entrarem em colapso, de maneira que não chegam à fase adulta. Apenas os machos são liberados na natureza para cruzar com as fêmeas selvagens, produzindo a descendência modificada.
Sobre isso, assinale a alternativa correta.
a) A transgenia fornece uma única estratégia de controle para todas as regiões do país, pois os machos se adaptam a todas as variantes de fêmeas.
b) As larvas transgênicas sugarão o sangue, mas suas picadas não transmitirão a doença para os seres humanos.
c) Os indivíduos picados pelos mosquitos transgênicos herdarão os genes modificados e diminuirão a propensão para desenvolver a dengue.
d) Os machos irão transmitir o gene alterado para as fêmeas que, também, expressarão a proteína em excesso, fazendo as células larvais entrarem em colapso.
e) Os machos não picam nem carregam o vírus, por isso foram escolhidos para serem modificados geneticamente com essa estratégia.
20. (UEPA) Leia o Texto abaixo para responder esta questão.
Por meio da técnica da CLONAGEM, foi feito o sequenciamento do gene da enzima catalase em ostra do mangue (Crassostrea rhizophorae), com o objetivo de contribuir para o desenvolvimento de indicadores de saneamento ambiental e saúde pública que possam ser utilizados para informar a comunidade e avaliar a qualidade de vida a partir de intervenções voltadas à proteção e recuperação de mananciais.
Sobre a técnica em destaque no Texto, afirma-se que:
a) Um óvulo é extraído de uma fêmea adulta de outra espécie conservando o seu núcleo.
b) Na ovelha Dolly, foram utilizadas células somáticas mamárias retiradas de um animal adulto.
c) O núcleo da célula mamária foi inserido no óvulo nucleado de outra fêmea que assim se tornou diploide.
d) O núcleo do óvulo de uma fêmea é inserido nas células da glândula mamária de outra fêmea.
e) Na ovelha Dolly, o núcleo do óvulo foi inserido na célula da glândula mamária, originando um clone do indivíduo que doou o núcleo.
 Direito de imagemGETTY IMAGES
Direito de imagemGETTY IMAGES Direito de imagemSCIENCE PHOTO LIBRARY
Direito de imagemSCIENCE PHOTO LIBRARY
 Direito de imagemGETTY IMAGES
Direito de imagemGETTY IMAGES Direito de imagemSCIENCE PHOTO LIBRARY
Direito de imagemSCIENCE PHOTO LIBRARY